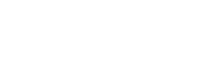Litijev naslednik
Od konca 90. let so baterije v moderni elektroniki skoraj brez izjeme litij-ionske, napredek pa je vsako leto težavnejši. Z naraščanjem njihove priljubljenosti in števila elektronskih naprav pa so se pojavili povsem netehnološki problemi virov litija, njegovega pridobivanja in uporabe kobalta, niklja in bakra kot nujnih pomočnikov. Pod litijem v periodnem sistemu najdemo natrij, ki se že uporablja v večjih sistemih.
Enota natrij-ionskih baterij v Hubeju na Kitajskem, ki lahko uskladišči 100 MWh energije. Slika: Hina Battery
Moderni pametni telefoni so računalniki v malem, ki so od legendarne Nokie 3310 za več velikostnih razredov zmogljivejši. Čeprav ima Googlov novi Pixel 16-milijonkrat več pomnilnika in 30-krat hitrejši procesor, zmore delovati s podobno avtonomijo kot stara nokia. A razlika ni posledica izjemnega napredka na področju baterij, temveč varčnosti komponent.
Morda delamo razvijalcem baterij krivico, če napredek zadnjih dveh desetletij pavšalno odpravimo kot neizjemnega, a v primerjavi z velikostnimi redi in velikimi izboljšavami procesorjev baterije res zaostajajo. Stara nokia ima baterijo s kapaciteto 1.000 mAh, ki je bila v zadnjih revizijah že litij-ionska (prve različice so bile še nikelj-kovinsko hidride), najnovejši tisoč evrov vreden pixel pa – 4.700 mAh. To je več, baterija je robustnejša in bolj dolgoživa, a ni milijonkrat več. Fizike se ne da prelisičiti.
Litij-ionske baterije so lastnoročno odpele moderni svet od kablov, a s prihodom električnih avtomobilov in nestanovitnih obnovljivih virov energije povpraševanje po njih skokovito narašča. V iskanje naslednikov litija nas tako ne sili zgolj želja po povečanju zmogljivosti, temveč okoljska in fizikalna nujnost. Litija v dostopni obliki morda sploh ni dovolj, da bi se ves svet elektrificiral. Po optimističnih scenarijih ga bo zmanjkalo v polovici stoletja, po pesimističnih še precej hitreje.
Zato se velja spomniti, kaj je bil glavni razlog za izbiro litija. Resda so v praksi pomembne zelo inženirske lastnosti, kot so mobilnost ionov, odpornost na spominski efekt, življenjska doba (merjena v številu ciklov), nazivna napetost in konični tokovi, a vse to bi teoretično lahko dosegli tudi s kakšno drugo kemijo, pa je na koncu zmagala litijeva. Litij je prva kovina v periodnem sistemu, torej ima zelo visoko razmerje med nabojem iona in maso, hkrati pa so ioni dovolj majhni, da imajo visoko mobilnost in sposobnost vstavitve (interkalacija) v gobasto elektrodo.
Litijev sosed v isti skupini je natrij, ki je seveda večji (0,102 nm namesto 0,076 nm) in težji (23 g/mol namesto 6,9 g/mol), a še vedno bistveno manjši od svinca, niklja ali kadmija. Hkrati sodi natrij med najpogostejše elemente na Zemlji, neomenjene vire pa ima praktično vsaka država z dostopom do morske vode, da sploh ne omenjamo drugih virov. Natrij je z gospodarskega in okoljskega vidika toliko primernejši od litija, da tudi slabše kemijske lastnosti – do razumne meje, seveda – ne bi predstavljale ovire.
Zamisel ni nova
Nápak bi pomislili, da so se raziskovalci z natrijevimi baterijami začeli ukvarjati nedavno, ko smo se zavedeli nepovratnosti elektrifikacije sveta in litijevih omejitev. Razvoj natrij-ionskih baterij se je začel že v 70. letih preteklega stoletja, približno istočasno kot litij-ionskih, a se dolgo ni premaknil. Litij-ionske baterije so kazale velike napredke in žele vso pozornost raziskovalne srenje, hkrati pa je bila tehnologija raziskovanja manj razvita. Elektroliti in katodni materiali so bili slabši, delo v brezvodnih komorah je bilo težje dosegljivo kot danes, baterije pa so imele nižjo nazivno napetost (pod 3 V) od litij-ionskih. Četudi je kemija obeh vrst baterij podobna, le nosilci naboja so drugi elementi, so bile natrij-ionske baterije deležne podpovprečnega zanimanja.
Velikost in masa natrijevega iona v primerjavi z litijevim pomenita, da bo energijska gostota vedno manjša, a to ni nepremostljiv problem. Le manjši del mase baterije odpade na nosilce naboja; pomembnejši so elektrodni materiali. Po drugi strani pa aluminij – še en sorazmerno poceni material – z litijem pri nizkih potencialih reagira, z natrijem pa ne, zato odpade potreba po dražjem bakru. Natrij-ionske baterije imajo še nekaj drugih prednosti. Ker natrij tvori bistveno več spojin s prehodnimi elementi (kakršen je kobalt) kot litij, imamo pri izbiri elektrodnega materiala več možnosti. Obetavne so spojine z nikljem, manganom, s kromom in z železom. Natrijevi ioni imajo hitro difuzijo, zato je moč izdelati baterije z visokimi koničnimi tokovi (in močmi). Natrij in njegove spojine so bolj ognjevarne kot litij, zato so tudi povsem napolnjene baterije manj nevarne.
Zanimanje za natrij-ionske baterije se je obnovilo po letu 2010, kar sovpada z razmahom električnih vozil. Ne le da bo količinsko potreba po baterijah za velikostni razred večja od potreb v potrošni elektroniki, pri vozilih so kupci bolj cenovno občutljivi. Do konca desetletja so specifične kapacitete presegale 200 mAh/g, večji problem pa je predstavljala dolgoživost, torej ohranjanje lastnosti po več ciklih polnjenja in praznjenja.
Pogled v notranjost
Zelo splošno smo o delovanju vseh vrst primarnih (ki se ne dajo napolniti) in sekundarnih baterij pisali pred desetletjem (Litij, ki poganja mobilni svet, Monitor 09/14). Osnove se niso spremenile, zato jih na tem mestu ne bomo ponavljali – in brez škode za razumevanje širše zgodbe lahko to poglavje preskočite.
Povejmo le, da baterije shranjujejo energijo, ker so v njih ločene snovi, ki bi želele med seboj reagirati. Ko jim reakcijo nadzorovano dopustimo, tečejo elektroni z negativno nabite anode na katodo. Ker jih vodimo skozi porabnik, lahko iz njih iztisnemo koristno delo. Hkrati morajo z anode na katodo potovati tudi pozitivno nabiti ioni, ki so v našem primeru natrijevi ioni; od tod imajo baterije tudi ime. Ioni potujejo skozi elektrolit. Reakcijo lahko obrnemo, tako da na anodo in katodo pritisnemo električno napetost, in tedaj bodo elektroni (in ioni) tekli v obratni smeri. Baterija se polni.
Pred natrijevo renesanso
Če bi morali časovno opredeliti renesanso natrij-ionskih baterij, bi izstopalo leto 2008. Tedaj se je v raziskovalni srenji močno povečalo število objavljenih člankov o tej temi, ki se odtlej hitro povečuje. A prvo navdušenje sega precej dlje v preteklost.
Medtem ko je γ-Al2O3 star material, odkrit že v 30. letih prejšnjega stoletja, so leta 1967 poročali o neobičajni mobilnosti natrijevih ionov v njem. Material namreč nima enostavne stehiometrične sestave, temveč ga gradijo aluminijev oksid, natrijev oksid in mešani oksid v različnih razmerjih. Ker zavzame posebno kristalno strukturo, v kateri so številne vrzeli, lahko natrijevi ioni švigajo po njih v svoji ravnini.
Drugo pomembno odkritje je natrij-žveplova kemija (NaS), ki jo odkril Ford v 60. letih. Te baterije uporabljajo γ-Al2O3 in tekoči natrij, na drugi elektrodi pa žveplo, ki se reducira v polisulfide. Celice delujejo pri visokih temperaturah med 300 in 350 °C. Izpeljanka te tehnologije so baterije ZEBRA (ZEolite Battery Research Africa), ki namesto žvepla uporabljajo nikljev klorid (in aluminijev klorid za znižanje tališča). A ko se je konec 70. let začel hitro dogajati razvoj litij-ionskih baterij, je natrij za tri desetletja utonil v pozabo. Začela se je natrijeva zima.
Primitivne natrij-žveplove in ZEBRA baterije iz 60. in 70. let, preden jih je zasenčil litij. Slika: B. L. Ellis, L. F. Nazar, Cur. Opin. Solid State Mater. Sci. 2012. 16, 168
V praksi udejanjiti ta teoretični koncept je vsej prej kot enostavno in predstavlja razliko med uspešnimi multinacionalkami in pokopanimi zagonskimi podjetji. Od baterije pričakujemo stabilnost v vseh pomenih besede. Preživeti mora več sto ali tisoč ciklov polnjenja in praznjenja brez večje izgube kapacitet, njena napetost mora biti podobna v širokem razponu bremen (baterija mora torej zagotavljati dovolj veliko moč, ne da bi se uničila), odporna mora biti na različne pogoje delovanja itd. Ob upoštevanju vseh zahtev se mnoštvo primernih materialov precej zoži.
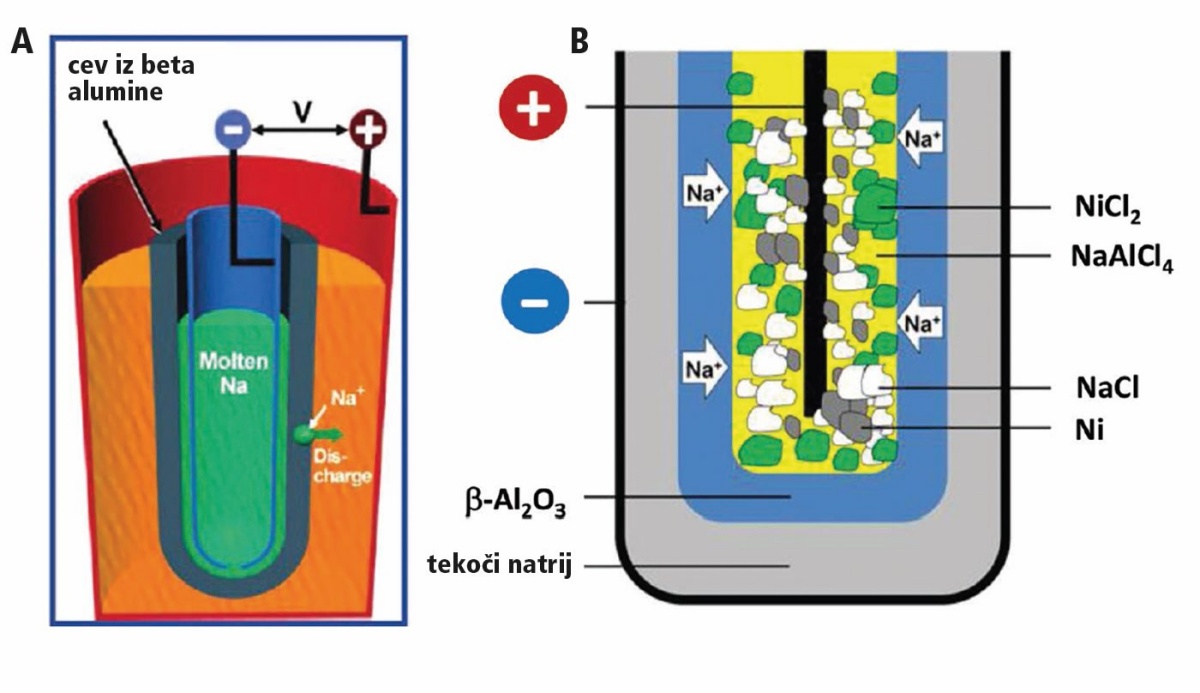
V natrij-ionskih baterijah so ti materiali drugačni kot pri litij-ionskih, ker imajo natrijevi ioni drugačne fizikalno-kemijske lastnosti. Kot anodni material se raziskujejo različne spojine, ki jih lahko razdelimo v tri velike skupine glede na način interakcije natrijevih ionov z elektrodo: vstavljanje (insertion), kemična pretvorba (conversion) in tvorba zlitin (alloying). V prvo skupino sodijo ogljikove spojine (trdi ogljik, grafen, ogljikov arzenid) in titanovi oksidi (npr. natrijev titanat). Oksidi, fosfidi in sulfidi kovin prehoda (transition metal oxides) sodelujejo v kemičnih pretvorbah, a ta vrsta zaradi velikih sprememb prostornine med reakcijo, kar lahko poškoduje baterije, ni posebej uporabna. Elementi 14. in 15. skupine periodnega sistema pa tvorijo zlitine, denimo svinec, bizmut, silicij, germanij, antimon, arzen in fosfor. V zlitinah je moč shraniti bistveno več natrijevih atomov kot z vstavljanjem v porozne materiale, a se pojavijo težave z nizko napetostjo in s spreminjanjem prostornine med reakcijo, česar ne želimo. V vseh primerih je torej v polni bateriji natrij shranjen v anodi, a z drugačno kemijo.
Tudi na katodi potrebujemo ustrezen material, ki bo omogočal reverzibilno vgradnjo natrijevih ionov. Trenutno so aktualne tri vrste teh materialov: oksidi, polianioni (fosfati, pirofosfati, fluorofosfati, oksikloridi) in superionski prevodniki. Pri vseh moramo zagotoviti čim manjšo spremembo strukture zaradi vgradnje natrija, kar je težje kot pri litiju, ker je natrij večji. Preprečiti je treba še izpostavljenost zraku ali vlagi, saj hitro nastane natrijev hidroksid, ki tvori izolacijsko plast. Priljubljeni materiali so tako natrij-železovi, natrij-nikljevi, natrij-manganovi, natrij-nikljevi oksidi, fosfati itd.
Elektrolit je često spregledan del baterij, a je vsaj tako pomemben kot anodni in katodni materiali. Od elektrolita zahtevamo kemično, elektrokemično in temperaturno stabilnost, dobro mobilnost ionov in slabo električno prevodnost, varnost in nizke proizvodne stroške. Povedano po domače: skozi elektrolit, naj bo tekoč ali trden, morajo čim lažje potovati natrijevi ioni. To dosežemo s premeteno izbiro topila, soli, ki jo v njem raztopimo, in morebitnih aditivov. Topilo mora biti torej inertno, nizkoviskozno, polarno z visoko dielektrično konstanto, medtem ko se mora sol v njem topiti in ne sme reagirati. Obetavna kombinacija so različna organska topila (na primer karbonatni estri), v katerih raztopimo enostavne anorganske natrijeve soli, denimo perklorate ali flurofosfate. Poleg klasičnih tekočih elektrolitov se raziskujejo tudi ionske tekočine in baterije s trdnim elektrolitom.
Shema sestavnih delov natrij-ionskih baterij. Slika: Yang-Kook Sun et al. Sodium-ion batteries: present and future. Chem Soc. Rev. 46, 12, 2017, 3485–3856
Proizvodnja je za vogalom
Razvoj natrij-ionskih baterij se je resda začel v ZDA, ključne ugotovitve so v preteklem desetletju prispevali japonski znanstveniki, a danes se je gonilo razvoja preselilo na Kitajsko. Lani je bilo na svetu v gradnji 20 tovarn za proizvodnjo takšnih baterij, izmed katerih jih je kar 16 na Kitajskem. To je razumljivo, saj Kitajska stavi na električno trojico (sončni paneli, baterije, vozila). Sama več kot 70 odstotkov litija uvaža, natrija pa ji ni treba.
Lani so Kitajci predstavili prve električne avtomobile, ki so uporabljali natrij-ionske baterije. Januarja letos se je že začela množična proizvodnja dveh modelov podjetij JMEV (Jiangling Motors Electric Vehicle), ki je v Renaultovi lasti, in Yiwei (ki je v solastništvu kitajske države in skupine Volkswagen). Oba modela imata serijsko vgrajene natrij-ionske baterije in deklarirana dosega okrog 250 kilometrov, saj imajo baterije energijsko gostoto okrog 150 Wh/kg. A ne gre le za avtomobile.
Na Kitajskem je maja letos začel delovati baterijski polnilnik Fulin, ki uporablja natrij-ionske baterije. Trenutno zmore shraniti 10 MWh energije, končni cilj pa je desetkrat več. Sestavljen je iz baterijskih celic s kapaciteto 210 Ah, ki se do 90 odstotkov napolnijo v 12 minutah. Sistem sestavlja 22.000 tovrstnih celic, učinkovitost (razmerje med energijo, ki jo dobimo pri praznjenju, in potrebno energijo za polnjenje) pa je okrog 92 odstotkov, kar je več od črpalnih elektrarn in primerljivo z litij-ionskimi baterijami (85–95 odstotkov).
Le nekaj tednov pozneje so v Hubeju predstavili sistem natrij-ionskih baterij, ki shrani 100 MWh električne energije. Tega sestavljajo baterije s kapaciteto 185 Ah in ima lastno 110-kilovoltno transformatorsko postajo. Proizvajalec zagotavlja, da baterije tudi pri temperaturah –20 °C dosegajo 85-odstotno učinkovitost in da jamčijo vsaj 1.500 ciklov, četudi temperature dosežejo 60 °C.
V prihodnjem letu naj bi na Kitajskem začeli proizvajati tudi natrij-ionske baterije manjšega formata, ki bi lahko bile primerne za prenosne naprave. Da bodo v praksi uporabne, bo treba še nekoliko povečati energijsko gostoto, da bo presegla 200 Wh/kg in se morebiti približala 300 Wh/kg. Dotlej bodo uporabne le v zelo varčnih napravah, kjer je cena najpomembnejši dejavnik. Kitajski CATL, ki je prvo množično proizvodnjo začel leta 2019, prav letos razvija drugo generacijo z energijsko gostoto 200 Wh/kg. Tudi BYD je letos začel dobro milijardo evrov težko investicijo v obrat za proizvodnjo natrij-ionskih baterij.
Zaostanek bo treba nadoknaditi
Fizikalni zaostanek natrij-ionskih baterij izvira iz fizikalno-kemijskih lastnosti natrijevih ionov in ga nikoli ne bomo mogli nadoknaditi, a to niti ni potrebno. Nova tehnologija se ni pojavila, da bi bila v vseh pogledih boljša od litij-ionskih baterij, temveč zato, ker obljublja cenejše, dostopnejše, morda tudi odpornejše in varnejše baterije. V najnovejšem telefonu sta resda pomembna vsak gram in vsaka minuta avtonomije, v ogromnih baterijskih kompleksih sredi Avstralije za uravnavanje proizvodnje in porabe električne energije pa sploh ne. Tam nekaj dodatnih kubičnih metrov in ton več kot odtehta nižja cena. Prostora imajo dovolj. Zdi se celo, da bodo natrij-ionske baterije omogočale večje konične moči (v W/kg) od litij-ionskih baterij.
Druga vrsta zaostanka pa je tehnološki. Izjemna pozornost, ki so jo raziskovalci posvetili litij-ionskim baterijah, je v dveh desetletjih pripeljala do komercialnega izdelka, nato pa je sledilo še 30 let izboljšav v praksi in nadaljnjega razvoja. Natrij-ionske baterije zaostajajo skoraj pol stoletja, saj so se resne raziskave začele šele v preteklem desetletju. Problemi, ki so pestili njihove starejše sestre in bili uspešno rešeni, se šele odpravljajo. Osnovni pristopi so enaki, zato nekaj prednosti imamo, a zaradi drugačne kemije potrebujemo druge materiale – ki jih je treba odkriti s preizkušanjem (to je zelo poenostavljeno rečeno) in v zadnjih letih čedalje bolj tudi s simulacijami. Trenutno največji problem predstavlja življenjska doba, torej odpornost na število ciklov, ker je pravzaprav edini resnično nespregledljivi problem, ki ga ni mogoče rešiti z več baterijami. Manjšo kapaciteto pač lahko presežemo s kopičenjem celic.
Raziskovalci so prepričani, da so natrij-ionske baterije prihodnost. Četudi je treba njihov optimizem vzeti z zrnom soli – navsezadnje govorijo o temi, ki jim neposredno daje kruh –, so povedne tudi poteze industrije. Na Kitajskem so že postavili prvi obrat za množično proizvodnjo novih baterij.
Električni avtomobil proizvajalca JAC uporablja natrij-ionske baterije podjetja Hina Battery. Prodajna cena vozila je približno 10.000 evrov.
Prihodnost bo bržkone pisana. Litij-ionske baterije bodo obstale, saj so preveč dobro razvita tehnologija, da bi jo zavrgli za slabši nadomestek, a ne za vse uporabe. Nobenega razloga ni, da bi uporabljali isto tehnologijo baterij v najdražjem iphonu in šestkrat cenejšem kitajskem telefonu, da ne omenjamo tovornjakov in baterijskih stabilizatorjev elektroenergetskega omrežja. Zgodila se bo specifikacija. Dražje mobilne naprave bodo uporabljale litij-ionsko tehnologijo, električna vozila odvisno od cene, poceni naprave in veliki hranilniki pa natrij-ionske.
Na pragu pa je tudi kvalitativna sprememba. Kot smo na tem mestu pisali že pred leti, korenitih sprememb v družbo ne prineseta odkritje niti komercializacija novih tehnologij, temveč njihova pocenitev do ravni, da si jih lahko privošči slehernik. Litij-ionske baterije so to omogočile potrošni elektroniki, zatika pa se jim pri električnih avtomobilih (cena baterije je znaten del vozila) in večjih namenih (spomnimo se še zidne baterije, ki jo je ponujala Tesla za električno neodvisnost gospodinjstev). Pomislimo, kaj vse bi bilo mogoče, če bi bile baterije stokrat cenejše in okolju prijaznejše. Ali bodo takšne prav natrij-ionske baterije, pa bomo videli čez desetletje ali dve.